 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
反应Zn(s)+Hg2Cl2(s)====2Hg(l)+Zn2+(aq)+2Cl-(aq)在25℃下,当各离子浓度均为1.0mol·dm-3时,测得电池电动势
反应Zn(s)+Hg2Cl2(s)====2Hg(l)+Zn2+(aq)+2Cl-(aq)在25℃下,当各离子浓度均为1.0mol·dm-3时,测得电池电动势为1.03V,当c(Cl-)=0.100mol·dm-3时,电动势为1.21V,此时c(Zn2+)为多少?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“反应Zn(s)+Hg2Cl2(s)====2Hg(l)+Zn…”相关的问题
更多“反应Zn(s)+Hg2Cl2(s)====2Hg(l)+Zn…”相关的问题
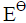 =0.2680V:
=0.2680V: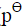 )|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)
)|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)
















