 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K时,已知如下电池的标准电动势=0.2680V: Pt|H2()|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)
298K时,已知如下电池的标准电动势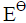 =0.2680V:
=0.2680V:
Pt|H2(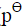 )|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)
)|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K时,已知如下电池的标准电动势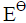 =0.2680V:
=0.2680V:
Pt|H2(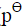 )|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)
)|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298K时,已知如下电池的标准电动势=0.2680V: Pt…”相关的问题
更多“298K时,已知如下电池的标准电动势=0.2680V: Pt…”相关的问题
当下列电池中的溶液是H=4.00时的缓冲溶液时,在25℃测得电池的电动势为0.209V。
(—)玻璃电极|H+(a=x) 当缓冲溶液由未知溶液代替时,测得电池电动势如下: (1)0.312V; (2)0.098V;(3)=0.017V。试计算每种溶液的pH值。
当缓冲溶液由未知溶液代替时,测得电池电动势如下: (1)0.312V; (2)0.098V;(3)=0.017V。试计算每种溶液的pH值。
已知下列反应的标准摩尔焓变,计算298K时SiC(s)的ΔH。
(1) C(s)+O2(g)====CO2(g),ΔH=-393.5 kJ·mol-
(2) Si(s)+CO2(g)====Si(s)+O2(g),△H=-989.2kJ/mol
A.7、60
B.4、60
C.5、60
D.6、60
A.同一种电池,体积越大,电动势也越大
B.电动势的大小表示电源把其他形式的能转化为电能的本领的大小
C.电路断开时,电源的非静电力做功为0,电动势并不为0
D.电路中电流越大,电源的非静力做功越多,电动势也越大
SiC是高温半导体、金属陶瓷和磨料等不可缺少的原料。现在以硅石(SiO2)和焦炭为原料制备SiC,反应为SiO2(s)+3C(石墨)===SiC(s)+2CO(g)
已知298K 时各物质的
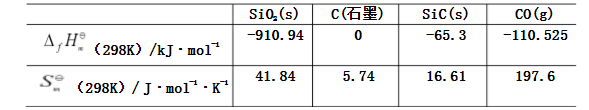
(1)计算在298K 时反应的 ,并判断298K 时能否获得SiC?
(2)估算在标准状态下生产SiC
将下列反应组成原电池(温度为298.15K):2Fe3++Cu====2Fe2++Cu2+
(1)计算原电池的标准电动势;(2)写出其电池符号;(3)指出正极、负极,并写出电极反应;(4)当Cu2+的浓度升到10mol·L-1时,原电池的电动势为多少?
A.0~30℃ 25℃
B.0~30℃ 20℃
C.0~25℃ 20℃
D.0~40℃ 25℃