 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用BaSO4灼烧法测定硫酸盐,水样中的()可影响硫酸钡的完全沉淀使结果偏低
A.氯化物
B.铬
C.硝酸银
D.悬浮物
 答案
答案
B、铬
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.氯化物
B.铬
C.硝酸银
D.悬浮物
 答案
答案
B、铬
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用BaSO4灼烧法测定硫酸盐,水样中的()可影响硫酸钡的完全…”相关的问题
更多“用BaSO4灼烧法测定硫酸盐,水样中的()可影响硫酸钡的完全…”相关的问题
用BaSO4重量法测定Ba2+的含量时,若有Fe3+、Mg2+、Cl-、NO3-等离子共存于沉淀溶液中,则______离子严重影响BaSO4沉淀的纯度。
A.0.19g
B.0.38g
C.0.16g
D.0.32g
称取0.5000g煤试样,灼烧并使其中硫全部氧化成为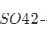 。处理成溶液并除去重金属离子后,加入0.05000mol·L-1BaCl220.00mL,使之生成BaSO4沉淀。过量的Ba2+用0.02500mol·L-1EDTA滴定,用去20.00mL。计算煤中硫的质量分数。
。处理成溶液并除去重金属离子后,加入0.05000mol·L-1BaCl220.00mL,使之生成BaSO4沉淀。过量的Ba2+用0.02500mol·L-1EDTA滴定,用去20.00mL。计算煤中硫的质量分数。
称取0.5000g煤试样,灼烧并使其中的硫完全氧化为SO42-。处理成溶液并除去重金属离子后,加入0.05000mol/L的BaCl2溶液20.00mL,使其生成BaSO4沉淀,过量的Ba2+用0.02500mol/L的EDTA标准溶液滴定,用去20.00mL。计算煤中硫的质量分数。
用沉淀称量法测定硫酸根含量时,如果称量式是BaSO4,换算因数是:()
A.0.1710
B.0.4116
C.0.5220
D.0.6201
用重量法测定试剂Na2HPO4·12H2O的纯度,首先是将试剂中的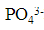 转化为MgNH4PO4·6H2O沉淀,然后灼烧成Mg2P2O7,为了使灼烧后所得的Mg2P2O7的称量误差小于0.1%,问至少应称取多少克试样?(已知相对分子质量:Na2HPO4·12H2O为358.1,MgP2O7为22.6,MgNH2PO4·6H2O为245.9)
转化为MgNH4PO4·6H2O沉淀,然后灼烧成Mg2P2O7,为了使灼烧后所得的Mg2P2O7的称量误差小于0.1%,问至少应称取多少克试样?(已知相对分子质量:Na2HPO4·12H2O为358.1,MgP2O7为22.6,MgNH2PO4·6H2O为245.9)
测定,测得吸光度列入表8-2。求该水样中镉的含量。
| 表8-2吸光度测定结果 | |||
| 编号 | 水样量/mL | 加入Cd(μg/mL) | 吸光度A |
| 1 2 3 4 | 20 20 20 20 | 0 1 2 4 | 0.042 0.080 0.116 0.190 |
用配位滴定法测定工业用水总硬度,取水样100.0mL,以铬黑T为指示剂,在pH=10的NH3-NH4Cl缓冲溶液中,以0.01000mol·L-1EDTA标准溶液滴定至溶液由紫红色变为纯蓝色即为终点,消耗EDTA标准溶液10.28mL,计算水样的总硬度(以CaOmg·L-1计)。