 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
用BaSO4重量法测定Ba2+的含量时,若有Fe3+、Mg2+、Cl-、等离子共存于沉淀溶液中,则______离子严重影响BaSO4沉淀
用BaSO4重量法测定Ba2+的含量时,若有Fe3+、Mg2+、Cl-、NO3-等离子共存于沉淀溶液中,则______离子严重影响BaSO4沉淀的纯度。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用BaSO4重量法测定Ba2+的含量时,若有Fe3+、Mg2+、Cl-、NO3-等离子共存于沉淀溶液中,则______离子严重影响BaSO4沉淀的纯度。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用BaSO4重量法测定Ba2+的含量时,若有Fe3+、Mg2…”相关的问题
更多“用BaSO4重量法测定Ba2+的含量时,若有Fe3+、Mg2…”相关的问题
用沉淀称量法测定硫酸根含量时,如果称量式是BaSO4,换算因数是:()
A.0.1710
B.0.4116
C.0.5220
D.0.6201
于100mL含有0.1000g Ba2+的溶液中,加入50mL 0.010mol·L-1H2SO4溶液,问溶液中还剩下多少克Ba2+?如沉淀用100mL纯水或100mL 0.010mol·L-1H2SO4溶液洗涤,假设洗涤时达到了沉淀平衡,问各损失BaSO4多少毫克?
A.(Ba2+)=c(SO4(2-))
B.(Ba2+)=c(SO4(2-))=[Ksp(BaSO4)]1/2
C.(Ba2+)≠c(SO4(2-)),c(Ba2+)·c(SO4(2-))=Ksp(BaSO4)
D.(Ba2+)≠c(SO4(2-)),c(Ba2+)·c(SO4(2-))≠Ksp(BaSO4)
称取0.5000g煤试样,灼烧并使其中硫全部氧化成为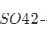 。处理成溶液并除去重金属离子后,加入0.05000mol·L-1BaCl220.00mL,使之生成BaSO4沉淀。过量的Ba2+用0.02500mol·L-1EDTA滴定,用去20.00mL。计算煤中硫的质量分数。
。处理成溶液并除去重金属离子后,加入0.05000mol·L-1BaCl220.00mL,使之生成BaSO4沉淀。过量的Ba2+用0.02500mol·L-1EDTA滴定,用去20.00mL。计算煤中硫的质量分数。
A.1.57
B.3.65
C.2.57
D.4.57