 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在101.325kPa下,HNO3、H2O系统的组成为: T/K 373 383 393 395 393 388 383 373
在101.325kPa下,HNO3、H2O系统的组成为:
| T/K | 373 | 383 | 393 | 395 | 393 | 388 | 383 | 373 | 358.5 |
| x(HNO3)液 y(HNO3)所 | 0.00 0.00 | 0.11 0.01 | 0.27 0.17 | 0.38 0.38 | 0.45 0.70 | 0.52 0.90 | 0.60 0.96 | 0.75 0.98 | 1.00 1.00 |

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“在101.325kPa下,HNO3、H2O系统的组成为: T…”相关的问题
更多“在101.325kPa下,HNO3、H2O系统的组成为: T…”相关的问题
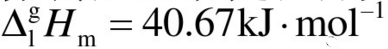 。
。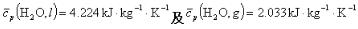 。今有101.325kPa下120℃的1kg过热水变成同样温度、压力下的水蒸气。设计可逆途径,并按可逆途径分别求出过程的△S及△G。
。今有101.325kPa下120℃的1kg过热水变成同样温度、压力下的水蒸气。设计可逆途径,并按可逆途径分别求出过程的△S及△G。















