 更多“在含有氯化银沉淀的溶液中加入氨水,沉淀的溶解度增大,这主要是…”相关的问题
更多“在含有氯化银沉淀的溶液中加入氨水,沉淀的溶解度增大,这主要是…”相关的问题
A.Ag+
B.Cd2+
C.Hg2+
D.Pb2+E.Cu2+
从含镍废催化剂中可回收镍,其流程如下: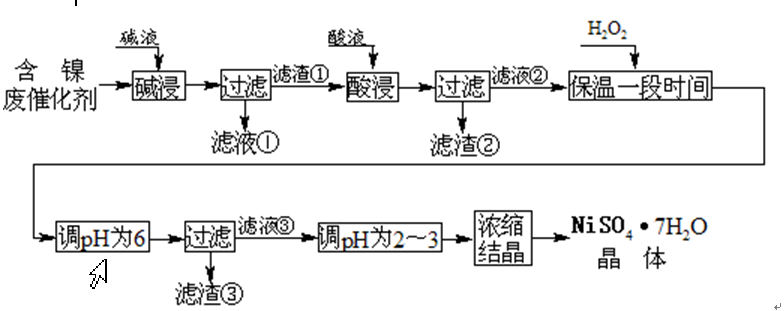 某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下
问题一、碱浸“的目的是除去()。
问题二、“酸浸”时所加入的酸是()(填化学式)。酸浸后,滤液②中可能含有的金属离子是()。
问题三、“调pH为2~3”的目的是()。
问题四、产品晶体中有时会混有少量绿矾(FeSO4•7H2O),可能是由于生产过程中()导致Fe2+未被完全氧化造成的。
问题五、NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料——NiOOH。该反应的离子方程式是()
①向溶液中先滴加过量硫酸铁溶液,产生红褐色沉淀;
②继续滴加过量的氯化钡溶液,产生白色沉淀。
下列说法正确的是()。
A.原溶液中一定存在的离子:Na+,SO42-,OH
B.原溶液中一定不存在的离子只有Cu2+
C.原溶液中可能存在的离子:SO42-,NO3-
D.红褐色沉淀的化学式为Fe(OH)2
正极材料为LiCoO2的锂离子电池被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
问题一、橄榄石型LiFePO4是一种潜在的锂离子电池正极材料,它可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
①共沉淀反应投料时,不将(NH4)2Fe(SO4)2和LiOH溶液直接混合的原因是()。
②共沉淀反应的化学方程式为()。
③高温成型前,常向LiFePO4中加入少量活性炭黑,其作用除了可以改善成型后的LiFePO4的导电性能外,还能()。
问题二、废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过以下实验方法回收钴、锂 。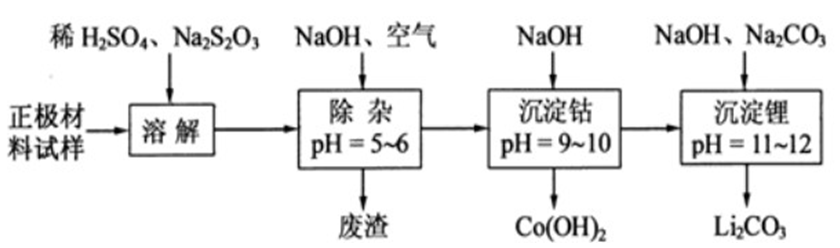
①在上述溶解过程中,S2O32ˉ被氧化成SO42ˉ,LiCoO2在溶解过程中反应的化学方程式为()。
②Co(OH)2在空气中加热时,固体残留率随温度的变化如以下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体成分为()。(填化学式);在350~400℃范围内,剩余固体成分为()。(填化学式) 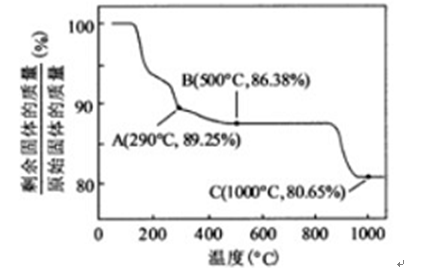

 如果结果不匹配,请
如果结果不匹配,请 
















