 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
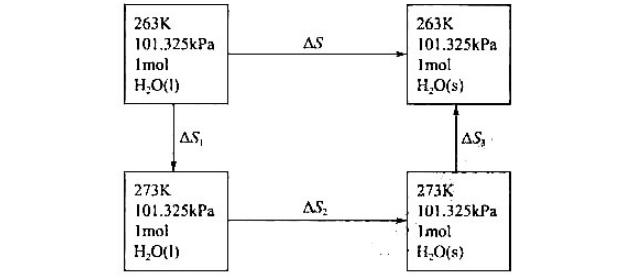
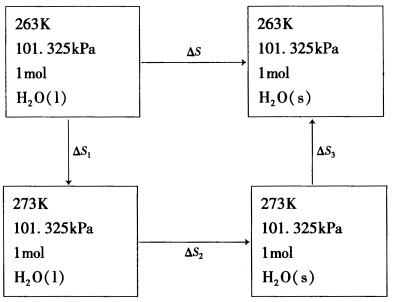
试计算263K和101.325kPa下1mol水凝结成冰这一过程的ΔS.ΔS环.和ΔS.并判断此过程是否为自发过程。
已知水和冰的热容分别为75.3J/(K.mol) 和273K时冰的熔化热为- 6025J/mol。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“试计算263K和101.325kPa下1mol水凝结成冰这一…”相关的问题
更多“试计算263K和101.325kPa下1mol水凝结成冰这一…”相关的问题
在293.15K及101.325kPa下,把半径为1×10-3m的汞滴分散成半径为1×10-9m的小汞滴,试计算此过程系统的表面吉布斯函数变为若干?已知293.15K时汞的表面张力为0.470N·m-1。
今有10mol液态水在其沸点(373.15K、101.325kPa)下,变为同温同压下的水蒸气,试计算该变化的Q、W和△U的值。已知水的摩尔气化焓变值△H=40.69kJ/mol。(水蒸气视为理想气体)。
1mol水在100℃,101.325kPa下向真空蒸发,变成100℃,101.325kPa的水蒸气,试计算此过程的△S系,△S环,并判断此过程是否自发过程。已知水的蒸发热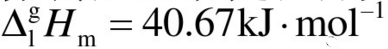 。
。
A.48000
B.34850
C.59620
D.29430
已知在101.325kPa下,水的沸点为100℃,其比蒸发焓△vaph=2257.4kJ·kg-1。已知液态水和水蒸气在100~120℃范围内的平均比定压热容分别为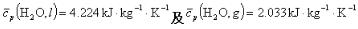 。今有101.325kPa下120℃的1kg过热水变成同样温度、压力下的水蒸气。设计可逆途径,并按可逆途径分别求出过程的△S及△G。
。今有101.325kPa下120℃的1kg过热水变成同样温度、压力下的水蒸气。设计可逆途径,并按可逆途径分别求出过程的△S及△G。