 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列说法正确的是()
A.25℃时,pH=12.0的KOH溶液中,由水电离出的(OH-)=10-12mol/L
B.25℃时,pH=12.0的KCN溶液中,由水电离出来的(OH-)=10-12mol/L
C.25℃时, 若某溶液水电离的氢离子浓度为10-5mol/L,则该溶液的pH为5
D.25℃时, 若某溶液水电离的氢离子浓度为10-11mol/L,则该溶液的pH为11
 答案
答案
AC
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.25℃时,pH=12.0的KOH溶液中,由水电离出的(OH-)=10-12mol/L
B.25℃时,pH=12.0的KCN溶液中,由水电离出来的(OH-)=10-12mol/L
C.25℃时, 若某溶液水电离的氢离子浓度为10-5mol/L,则该溶液的pH为5
D.25℃时, 若某溶液水电离的氢离子浓度为10-11mol/L,则该溶液的pH为11
 答案
答案
AC
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列说法正确的是()”相关的问题
更多“下列说法正确的是()”相关的问题
A.1 mol月球背面的氦-3(3He)含有质子为2NA
B.标准状况下,22.4 L甲烷和1 mol Cl2反应后的混合物中含有氯原子数小于2NA
C.2 mol SO2与1 mol O2充分反应,转移的电子数为4NA
D.25 ℃时,1 L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA
用NA代表阿伏加德罗常数的值,下列说法正确的是()。
A.
所含共价键数目均为0.4NA的白磷(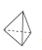 )和甲烷的物质的量相等
)和甲烷的物质的量相等
B.1molNa2O2与足量CO2充分反应转移的电子数目为2N
C.25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH﹣数目为0.2NA
D.常温下,向1L0.1mol•L﹣1醋酸钠溶液中加入醋酸至中性,则溶液中CH3COO﹣的数目为0.1NA
A.用含0.1molFeCl3的饱和溶液制取Fe(OH)3胶体得0.1NA个胶粒
B.将含有NA个Al3+的AlCl3溶液完全蒸干,可得到1mol的固体AlCl3
C.电解法精炼铜,当电路中有0.2NA个电子转移时,阳极的质量一定减轻6.4g
D.25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目约为0.1NA
25℃时,向20mL0.1mol/LHAuCl4溶液中滴加0.1mol/LNaOH溶液,滴定曲线如图1所示,含氯微粒的物质的量分数(δ),则下列说法不正确的是()。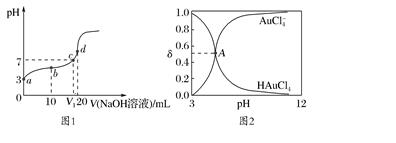
A.图2中A点对应溶液的pH约为5
B.b点对应溶液中:c(Na+)>c(AuCl4﹣)
C.d点对应溶液中:c(OH﹣)﹣c(H+)=c(HAuCl4)
D.滴定过程中,n(HAuCl4)与n(AuCl4﹣)之和保持不变
A.密闭容器中2 mol NO与1 mol O2充分反应,产物分子的数目为2NA
B.25℃,pH=13的NaOH溶液中含有OH-的数目为 0.1NA
C.标准状况下,22.4 L CCl4含CCl4分子数为NA
D.标准状况下,22.4L N2与CO混合气体的质量为28g
A.囊材浓度以25%~5%为宜
B.成囊时pH应调至4.0~4.5
C.成囊时温度应为50~55℃
D.甲醛固化时温度在10℃-15℃
E.甲醛固化时pH应调至8~9
当下列电池中的溶液是H=4.00时的缓冲溶液时,在25℃测得电池的电动势为0.209V。
(—)玻璃电极|H+(a=x) 当缓冲溶液由未知溶液代替时,测得电池电动势如下: (1)0.312V; (2)0.098V;(3)=0.017V。试计算每种溶液的pH值。
当缓冲溶液由未知溶液代替时,测得电池电动势如下: (1)0.312V; (2)0.098V;(3)=0.017V。试计算每种溶液的pH值。
A.1 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2NA
B.12 g石墨烯(单层石墨)中含有六元环的个数0.5NA
C.25 ℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA
D.1 mol的羟基与1 mol的氢氧根离子所含电子数均为9NA
A.1.0 L 1.0 mo1·L−1的NaAlO2水溶液中含有的氧原子数为2NA
B.12g石墨烯(单层石墨)中含有六元环的个数为0.5NA
C.25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA
D.1 mol的羟基与1 mol的氢氧根离子所含电子数均为9NA
A.离解度增大,H+浓度减小
B.离解度增不变,H+浓度减小
C.酸的浓度减小,pH增大
D.酸的浓度减小,pH不变
E.酸的浓度减小,离解度不变