题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
你在进行服从与惩罚的实验时,以大鼠为被惩罚对象,希望观察被试对大鼠的电击力度的变化及其影响因素。你认为在进行实验之前,需要做好哪些伦理规范上的准备工作()
A.寻求研究替代方案,尽量不使用动物实验,同时也实现研究目标
B.做好伦理审批,详细介绍实验方案
C.实验过程中尽力减少大鼠的痛苦
D.实验结束后,为被试提供必要的心理干预
E.实验结束后,为大鼠提供必要的帮助,缓解其痛苦
 答案
答案
E、实验结束后,为大鼠提供必要的帮助,缓解其痛苦
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“你在进行服从与惩罚的实验时,以大鼠为被惩罚对象,希望观察被试…”相关的问题
更多“你在进行服从与惩罚的实验时,以大鼠为被惩罚对象,希望观察被试…”相关的问题
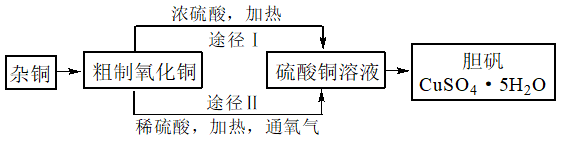
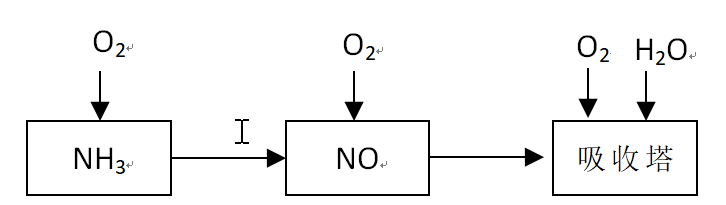 某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。
某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)。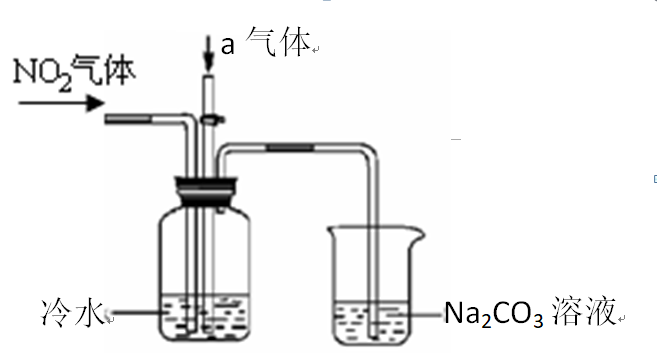
 N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。
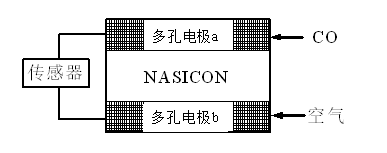
N2O4(g)的平衡常数K=()。假设NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为()。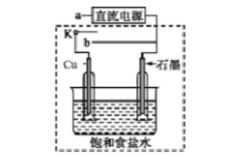 ①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。
①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。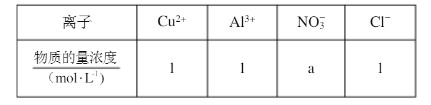 用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。
用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。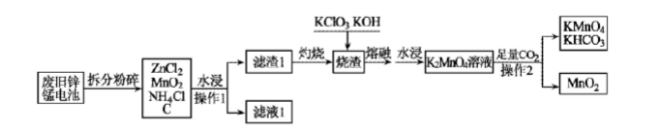 (1)K+的结构示意图为()。
(1)K+的结构示意图为()。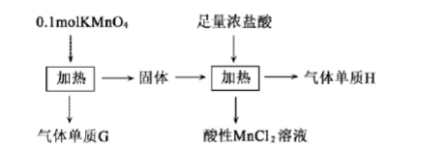 A、G与H均为氧化产物
A、G与H均为氧化产物